主办:佑安肝病感染病专科医疗联盟遗传代谢性肝病专业委员会;中华医学会肝病学分会遗传代谢性肝病协作组
总编辑:段钟平
本期责任主编:吴东波
执行编辑:郑素军,梁晨,侯维
本期目录
一、主编致辞
二、学术进展
三、临床资
四、联系方式
月报撰稿及简评专家主要为中华医学会肝病学分会遗传代谢性肝病协作组、佑安肝病感染病专科医疗联盟遗传代谢性肝病专业委员会,以及其他相关领域专家。
“学术进展”:速览最新重要文献,了解遗传代谢性肝病的科研前沿!
“临床资讯”:提供典型病例、名家讲座等信息,共享临床诊治奥妙!
一、主编致辞
家族性肝内胆汁淤积(familial intrahepatic cholestasis)是一组常染色体隐性遗传病,以肝内胆汁淤积为主要表现,可反复发生或持续进展。持续进展的病例又称进行性家族性肝内胆汁淤积(progressive familial intrahepatic cholestasis,PFIC),轻症病例可表现为良性复发性肝内胆汁淤积(benign recurrent intrahepatic cholestasis,BRIC)。部分BRIC病例反复发作,也可最终进展为PFIC。
根据致病基因不同,既往将PFIC分为3型:1型是由编码FIC1的ATP8B1基因突变所致;2型是由编码胆盐输出泵(bile salt export pump,BSEP)的ABCB11基因突变所致;3型是由编码多药耐药蛋白3(multidrugresistance protein 3,MDR3)的ABCB4基因突变所致。近年来随着研究的深入,逐步发现了由TJP [(编码紧密连接蛋白2(tight junction protein-2,TJP2),位于9号染色体],NR1H4[(编码法尼醇受体(farnesoid X receptor,FXR),位于12号染色体]及MYO5B(编码肌球蛋白VB,位于18号染色体)等其他基因突变引起的胆汁淤积。
本期报道的是一例ATP8B1基因突变所致BRIC 1型患者,ATP8B1缺乏可表现为持久性(PFIC 1)或偶发性(BRIC 1)胆汁淤积。
PFIC 1型通常表现在新生儿期,并伴有黄疸和生长迟缓。脂肪吸收不良往往导致脂溶性维生素缺乏。患者通常发展为终末期肝病,通常从婴儿期到青春期。
BRIC 1的特点是出现胆汁淤积,并伴有严重的瘙痒。第一次出现症状通常在儿童和青少年早期,但也有在婴儿期或中年后期才出现症状的报道。每次胆汁淤积症发作都会持续几周到几个月。在症状期之间,患者完全无症状数月至数年。症状发作可能与病毒感染有关。对于年龄较大的人(≥14岁),胆汁淤积症发作的频率通常会降低。
除了胆汁淤积外,ATP8B1缺乏症的患者还可能出现肝外症状,如腹泻、胰腺炎、听力问题和汗液氯离子浓度升高。
ATP8B1缺乏症的实验室表现主要表现为严重胆汁淤积(血清胆盐、胆红素和转氨酶水平升高)和谷氨酰转肽酶(GGT)水平低的特征。组织学上,有小管状胆汁淤积伴粗颗粒状胆汁。在PFIC 1中,最终会出现纤维化和肝硬化。在BRIC 1中,有胆汁淤积,没有纤维化的迹象,在发作之间肝活检正常。
PFIC 1和BRIC 1是一个疾病的不同程度的表现,PFIC 1是较严重表现形式,而BRIC 1是较温和的形式。最初诊断为BRIC的患者偶尔会发展为持续和进展的胆汁淤积。
本期月报介绍的这例患者,以胆红素升高、GGT正常为主要表现,依据家族史、病理及基因检测明确诊断。通过对该病例的分析,以期临床医师提高对BRIC的认识,对于原因不明的胆汁淤积,需拓宽思路,对于有家族史及年轻的患者应积极进行相关基因检测,警惕遗传代谢疾病等罕见病存在。

侯维
首都医科大学附属北京佑安医院,肝病中心一科,主任医师
中华医学会感染病学分会,青年委员
北京感染病学分会,委员
北京医学会肝病学分会,青年委员
二、学术进展
Pubmed最新重要文献速览(长按文末二维码或“阅读原文”可下载)
1.靶向区域测序和外显子测序用于遗传代谢性肝病(The Journal of pediatrics,2023,IF=5.10; Q1区)
2.胆盐输出泵缺陷症基因与表型关系(JHEP reports : innovation in hepatology,2023,IF=8.30; Q1区)
3.诊断抗体诱导的胆盐输出泵缺陷的新型无创方法(JHEP reports : innovation in hepatology,2023,IF=8.30; Q1区)
4.AAV基因治疗婴幼儿进行性家族性肝内胆汁淤积症3型小鼠模型(JHEP reports : innovation in hepatology,2023,IF=8.30; Q1区)
5.通过二代测序对 166 名肝内胆汁淤积儿童进行诊断并发现了新的致病基因(Hepatology International,2023,IF=6.60; Q1区)
6.胆盐输出泵缺陷症患者的肝脏结局:一项回顾性队列研究的结果(Hepatology communications,2023,IF=5.10; Q2区)
7.系统综述:治疗胆汁淤积性瘙痒(Therapeutic advances in gastroenterology,2023, IF=4.20; Q2区)
8.持续到成年的儿童胆汁淤积性肝病(Journal of clinical gastroenterology,2023,IF=2.90; Q3区)
9.病例汇编和文献回顾:进行性家族性肝内胆汁淤积症的内外科治疗(Children,2023,IF=2.40; Q2区)
10.不同基因型的进行性家族性肝内胆汁淤积症胆道分流术后的结局(Frontiers in surgery,2023,IF=1.80; Q3区)
三、临床资讯
3.1 病例分享
患者冯某某,男性,16岁,因“皮肤、巩膜黄染3月”于2023年2月22日就诊。
现病史:患者3月前因发热口服感康、999感冒冲剂等出现皮肤、巩膜黄染,伴乏力、食欲不振,无恶性、呕吐,无灰白便及腹痛,未予重视,未就诊。1月前在当地医院查TBIL 210µmol/l,DBIL 180µmol/L,PTA 95%,GGT 24U/L,ALP 216U/L,ALT 23U/L,AST 22U/L,MRCP 未见异常。予保肝、退黄治疗,大便转为灰白色,伴皮肤瘙痒,2周前行血浆置换及胆红素吸附,患者黄疸无下降,食欲无好转。1周前查WBC 11×109/L,HGB 128g/L,PLT339×109/L,予醋酸泼尼松龙40mg qd治疗3天,改用20mg治疗3天,为进一步诊治入院。
既往史及家族史:既往体健,生长发育无特殊。父母体健,其妹妹体健,姐姐幼年因反复黄疸在当地医院住院,以直接胆红素升高为主,GGT及ALP正常,PTA正常,因合并腰椎结核最终因多器官衰竭于17岁死亡。
入院查体:消瘦,身高:4250px,体重:47kg,皮肤巩膜黄染,可及皮肤抓痕,心肺阴性,腹软,中上腹压痛阳性,反跳痛阴性,移动性浊音阴性,双下肢无水肿。
入院后完善检查:血常规:WBC 17.4×109/L,HGB 95g/L,PLT 435×109/L,N% 82%。肝肾功能:TBIL 424 µmol/l,DBIL 351µmol/L,GGT 25U/L,ALP 257U/L,ALT 15U/L,AST 19U/L,ALB 32g/L,TBA139µmol/l,CREA 54µmol/L,凝血项:PTA 87%,心肌酶谱正常,乳酸正常,铜蓝蛋白、自身免疫抗体正常;嗜肝病毒检测(HAV、HBV、HCV、HEV、CMV、EBV)阴性,AFP:正常。免疫球蛋白:IgG 9.68g/L。血糖、血脂、肌酸激酶正常。
心脏彩超:三尖瓣返流(少量)
肝弹性硬度值:8.7kpa
B超:胆囊充盈不佳。
胃镜:慢性浅表性胃炎
增强CT:肝脏未见明确病变,胆囊未见充盈,左肾钙化灶
肝穿病理:肉眼所见:灰褐色穿刺组织1条,长1.6cm,直径5px。镜下所见:切片内共见14个中小汇管区,间质轻度单个核细胞浸润,小胆管,门脉及动脉保留,周边带少数细胆管增生。小叶结构保留,中心性毛细胆管淤胆,3带、2带为主,肝细胞未见明显肿胀,CK7免疫染色,中心带肝细胞浆时呈阳性。 病理诊断:(肝穿)肝内单纯性胆汁淤积,建议行基因检测除外良性复发性肝内胆汁游积(BRIC)。免疫组化:HBsAg (-);HBcAg (-);CK7 (胆管+); CK19(胆管+); MUM1(散在+);特殊染色:铁(Perls法,-)。
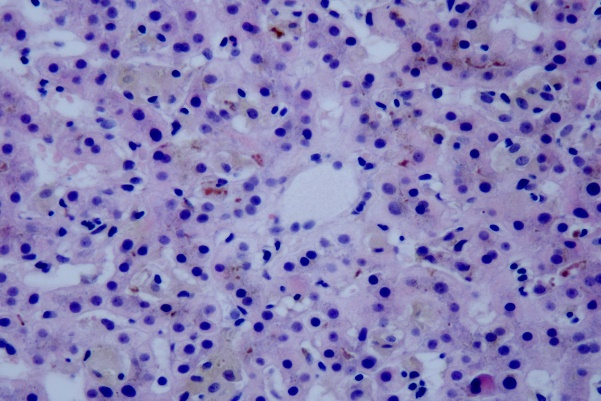
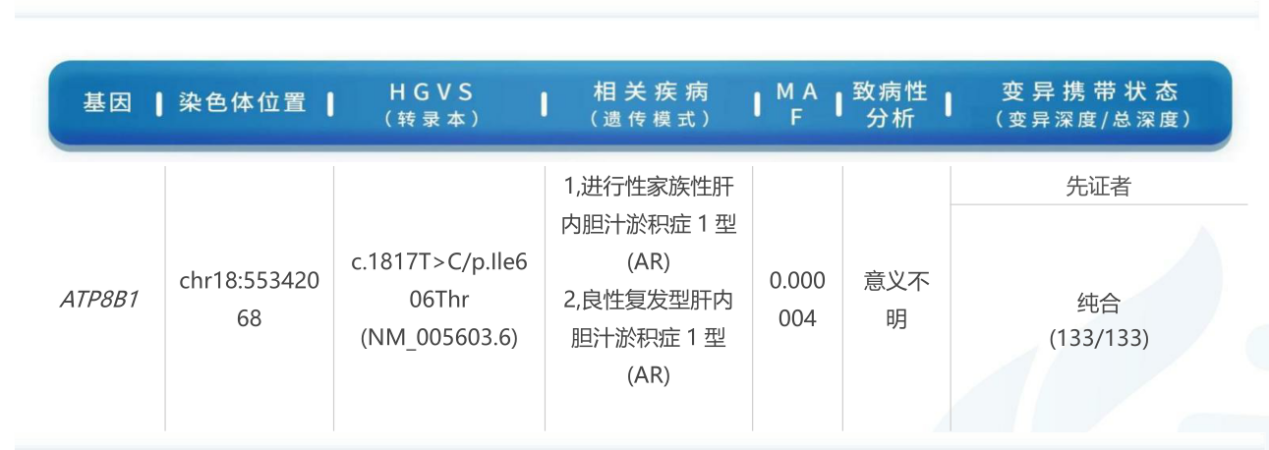
基因检测:在ATP8B1基因发现一处纯合变异:c.1817T>C/p.Ile606Thr (NM_005603.6)
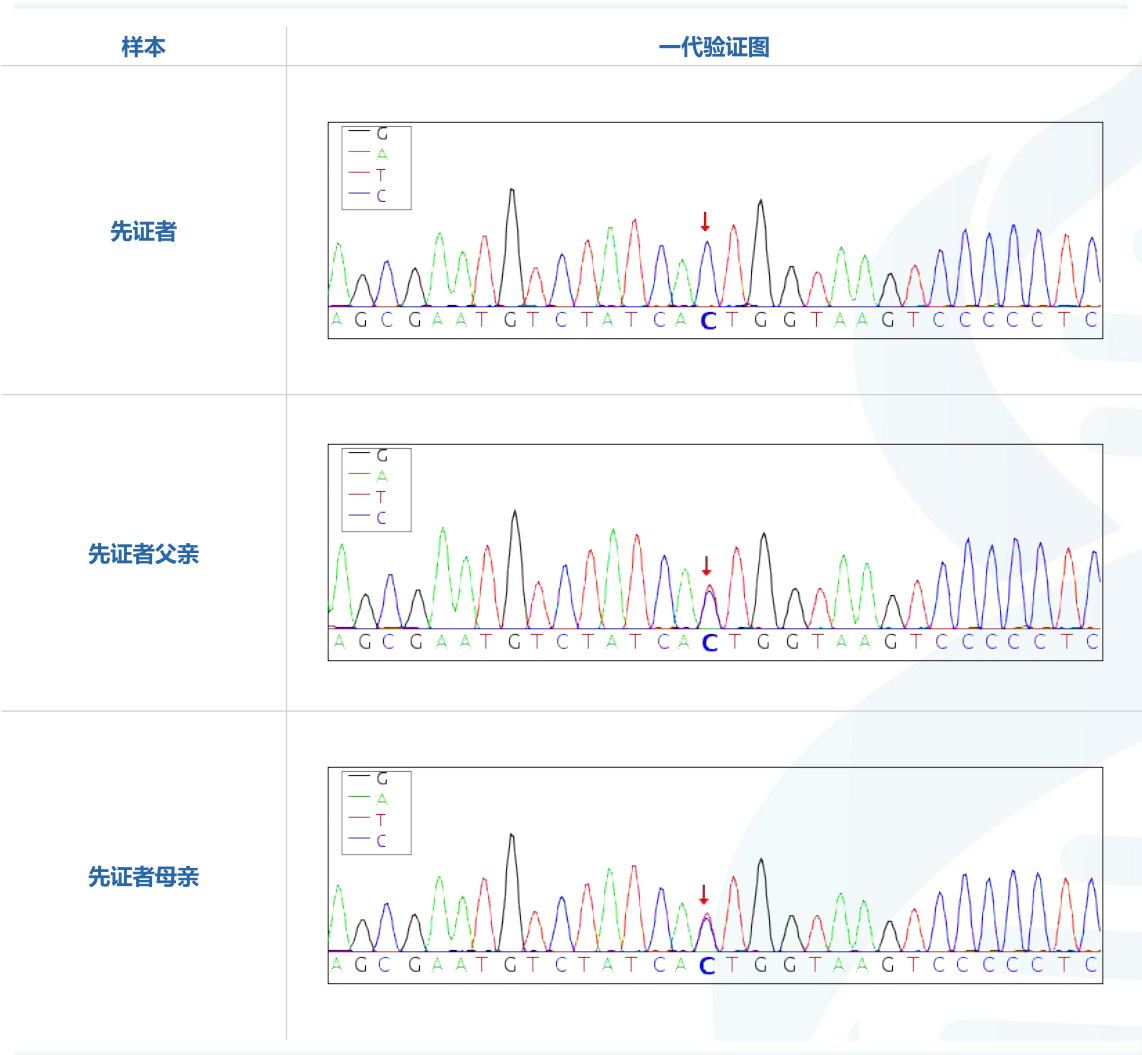
先证者父母行基因检测后提示先证者c.1817T>C分别来自父亲及母亲。

诊断:良性复发性肝内胆汁淤积(BRIC)
治疗:口服熊去氧胆酸250mg bid
随访:患者治疗3月后复查肝功能完全恢复正常,体重升至57kg。
3.2 供稿专家简介

王征
首都医科大学附属北京佑安医院,肝病中心一科,副主任医师
主要研究方向为"遗传代谢性肝病"
四、联系方式
▶投稿邮箱:yichuandaixie2020@163.com(用于征集典型病例、PPT或委员会动态信息)
▶联系电话:010-63291007
▶联系地址:北京市丰台区右安门外西头条8号佑安医院D楼(南入口)405房间

